L'anno scorso ha segnato il quarantesimo anniversario della comparsa sulla scena mondiale di un virus che ha cambiato la storia dell’umanità, provocando quasi 35 milioni di morti: l’HIV, il virus dell’immunodeficienza umana.
Un virus che grazie agli sforzi di ricercatori di tutto il mondo abbiamo imparato a conoscere e a controllare con i farmaci e che speriamo in futuro, grazie ai progressi della ricerca, di contrastare più efficacemente grazie a un vaccino o a nuove terapie.
Ma proprio la ricerca, in cui la Fondazione Telethon ha avuto un ruolo da protagonista, ha messo in luce anche un'altra faccia di questo temibile virus: la possibilità di manipolarlo in laboratorio e trasformarlo in un farmaco di precisione, per la terapia genica di malattie genetiche rare e tumori. In occasione della Giornata mondiale per la lotta all’AIDS, scopriamo insieme le tappe di questa affascinante storia.
- 1981: una strana sindrome viene descritta negli Usa
- 1982: coniato il termine AIDS
- 1983: scoperto il virus responsabile dell’AIDS
- 1985: la prima vittima celebre dell’AIDS
- Ritratto di un nuovo agente patogeno
- 1996, un anno di svolta per la terapia anti-HIV
- Un’altra faccia per il virus
- L’inizio di una nuova medicina
- I farmaci basati su vettori derivati da HIV
- I numeri dell’HIV/AIDS oggi
1981: una strana sindrome viene descritta negli Usa
Nell’estate del 1981 prima i Centers for Disease Control and Prevention (CDC) di Atlanta, poi il quotidiano New York Times, descrivono uno strano fenomeno riscontrato in giovani uomini omosessuali, apparentemente in buona salute: l’insorgenza di polmoniti e tumori piuttosto rari, noti per colpire soprattutto persone con un sistema immunitario compromesso. Nel giro di pochi anni tutti questi pazienti muoiono in maniera inspiegabile.
1982: coniato il termine AIDS
Questi strani casi aumentano e si fa strada l’idea di essere di fronte a una nuova malattia, probabilmente infettiva ma di cui si ignora la modalità di trasmissione. Inizialmente si pensa colpisca solo gli omosessuali, ma presto i fatti lo smentiscono: nello stesso anno, per esempio, muore un bambino con emofilia a seguito di una trasfusione infetta e si registra il primo caso di trasmissione da madre a feto. La malattia inizialmente chiamata “immunodeficienza gay-correlata” viene definita AIDS, sindrome da immunodeficienza acquisita.
1983: scoperto il virus responsabile dell’AIDS
Il 20 maggio due virologi dell’Istituto Pasteur di Parigi, Luc Montagnier e Françoise Barré-Sinoussi, descrivono sulla rivista Science un nuovo virus candidato come agente responsabile dell’AIDS. È un retrovirus, ha cioè la peculiarità di poter integrare stabilmente il proprio patrimonio genetico, a base di RNA, in quello della cellula ospite grazie a due enzimi: la trascrittasi inversa, che converte l’RNA virale in DNA, e l’integrasi, che lo inserisce in quello della cellula infettata. Una strategia conveniente per il virus, perché il suo patrimonio genetico non viene mai eliminato e fa da base per la produzione di nuove particelle virali per tutta la vita della cellula ospite. I risultati sono confermati l’anno dopo da Robert Gallo dell’Università del Maryland, che nonostante una lunga battaglia legale sulla paternità della scoperta sarà escluso dal premio Nobel per la Medicina assegnato nel 2008 a Montagnier e Barrè-Sinoussi.
1985: la prima vittima celebre dell’AIDS
Il 2 ottobre muore l’attore Rock Hudson, pochi giorni dopo aver dichiarato pubblicamente di essere affetto da AIDS: è la prima “vittima celebre”, l’impatto mediatico è enorme e sottolinea l’impotenza di fronte a quella che è ormai una pandemia. Sei anni dopo, il 24 novembre 1991, sarà la volta del leader dei Queen Freddie Mercury. Altre persone note scomparse a causa dell’AIDS, sviluppata per motivi molto diversi, saranno nel 1992 lo scrittore di fantascienza Isaac Asimov e l’attore Anthony Perkins e, nel 1993, il ballerino Rudolf Nureyev e il tennista Arthur Ashe. In Italia, dimenticato da tutti, morirà anche il portiere del Napoli Giuliano Giuliani (1996).
Ritratto di un nuovo agente patogeno
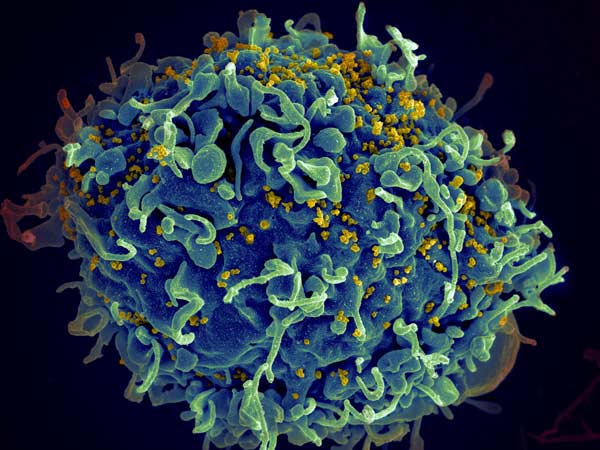
Ricercatori di tutto il mondo sono al lavoro per comprendere meglio il comportamento del nuovo virus. Emerge presto che non è l’HIV in sé a uccidere, ma la sindrome che si instaura dopo che particolari cellule del sistema immunitario vengono distrutte. Come per ogni virus, il suo obiettivo è replicarsi e per farlo ha bisogno di una cellula ospite. Il suo bersaglio sono i linfociti T CD4 helper, globuli bianchi che si attivano in risposta alle nuove infezioni da virus e che ne conservano un ricordo per difendere l’organismo in futuro. Nell’infezione da HIV i CD4, pur attivandosi, sono presi di mira dal virus e non sono in grado di mantenere un ricordo dell’infezione. Se lasciato a replicarsi indisturbato, nel tempo HIV indebolisce irrimediabilmente il sistema immunitario. Quando il valore dei CD4, che normalmente è di 500-1200 per ml di sangue, scende sotto 200 si parla di AIDS conclamata, che mette l’individuo a rischio di malattie “opportunistiche”, che si verificano cioè soltanto quando il sistema immunitario è gravemente compromesso. Sono queste a mettere in pericolo di vita e non l’infezione in sé.
Celeberrima la scena del film del 1991 “Philadelphia” in cui il protagonista, interpretato da Tom Hanks, viene “scoperto” dai suoi colleghi quando sul suo viso compaiono le tipiche lesioni del sarcoma di Kaposi, un raro tumore molto diffuso invece tra i malati di AIDS.
1996, un anno di svolta per la terapia anti-HIV
Dopo anni di tentativi e sforzi collettivi, si comincia a vedere la luce in fondo al tunnel per quanto riguarda il controllo dell’infezione, come annunciato alla XI Conferenza Internazionale sull’Aids di Vancouver. I primi farmaci anti-retrovirali, che bloccano cioè la replicazione del virus, si dimostrano in grado di tenere l’infezione sotto controllo, soprattutto se usati in combinazione. Agendo su bersagli molecolari diversi, infatti, permettono di ovviare al grosso problema dell’estrema tendenza di HIV a mutare, per sfuggire al sistema immunitario. La terapia combinata (Highly Active Anti-Retroviral Therapy, o HAART) è tuttoggi lo standard di cura: attualmente disponiamo di 20 tipi diversi di farmaci antiretrovirali e anche la tollerabilità è migliorata, anche se rimangono comunque effetti collaterali, variabili da individuo a individuo (maggiori dettagli sul sito della Lega Italiana Lotta all’AIDS).
Un’altra faccia per il virus
Nello stesso anno per la prima volta viene mostrata un’altra faccia di HIV, che dà un nuovo impulso a un settore ancora emergente, quello della terapia genica: l’idea di sfruttare i virus come trasportatori di versioni sane di geni difettosi, per esempio per curare malattie genetiche rare.
Al Salk Institute for Biological Studies di La Jolla, il centro di ricerca californiano fondato dall’inventore del vaccino anti-polio Jonas Salk, un giovane ricercatore italiano “prestato” agli Usa, Luigi Naldini, pubblica su Science uno studio che negli anni successivi si rivelerà fondamentale.
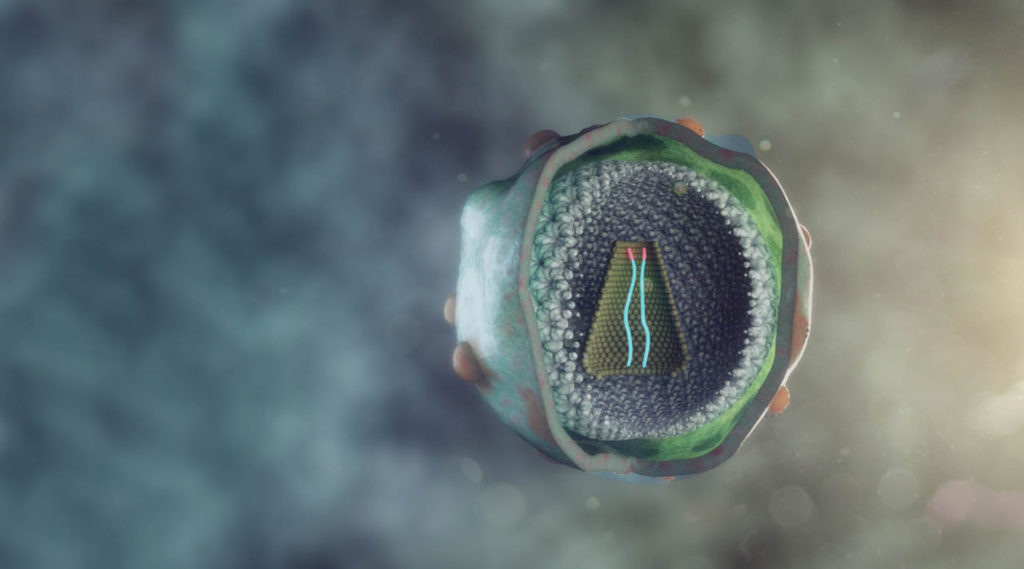
Dimostra che proprio per la sua capacità di inserirsi stabilmente nel DNA della cellula ospite HIV può essere la base di partenza per costruire nuovi vettori per la terapia genica. Privato di alcune porzioni, può essere usato per trasportare materiale genetico di interesse anche nelle cellule più “restie” a essere corrette, senza provocare l’infezione. Un simile vantaggio sarebbe prezioso, perché permetterebbe di introdurre stabilmente geni di interesse nella maggior parte dei tessuti che normalmente non sono in attiva replicazione.
L’inizio di una nuova medicina
Inizialmente la comunità scientifica accoglie l’idea in modo ambivalente: molto interessante dal punto di vista scientifico, ma troppo pericolosa per essere messa in pratica. Come ha ricordato lo stesso Naldini in questa intervista, «il lavoro del 1996 è stato indubbiamente uno spartiacque, ma il percorso successivo non è stato facile. Ci sono state battute d’arresto dovute ad applicazioni premature della terapia genica nell’uomo, oltre a resistenze culturali da parte della comunità scientifica stessa all’idea di impiegare vettori derivati da HIV per curare malattie umane. La Fondazione Telethon ha avuto la lungimiranza di crederci ed è per questo che dopo il mio definitivo rientro in Italia all’inizio del 2000 ho iniziato a collaborare con l’Istituto San Raffaele-Telethon (SR-Tiget) di Milano, allora diretto da Maria Grazia Roncarolo, per trasformare quei risultati in opportunità concrete di cura».
«La Fondazione Telethon ha avuto la lungimiranza di credere nella terapia genica»
Luigi Naldini, direttore SR-Tiget
Smontato pezzo per pezzo HIV - del virus originale non resta che un 10 per cento - si rivelerà effettivamente un vettore molto interessante, in termini di efficacia e sicurezza. Nel 2013 i ricercatori dell’SR-Tiget di Milano, diretto da Naldini a partire dal 2008, annunciano i primi risultati positivi delle terapia genica con vettori derivati da HIV in due gravi malattie genetiche dell’infanzia. Per la leucodistrofia metacromatica, la terapia genica è stata approvata come farmaco in Europa alla fine del 2020, con il nome di Libmeldy.
I farmaci basati su vettori derivati da HIV
Attualmente i vettori derivati dal virus HIV, detti lentivirali, sono al secondo posto dopo quelli di tipo AAV (adeno-associato) tra quelli utilizzati per il trasferimento di geni terapeutici e rappresentano circa un terzo del totale (fonte Cell & Gene Therapy Dashboard Informa, aprile 2021).
Delle 12 terapie geniche che hanno finora ottenuto l’autorizzazione in Europa, cinque si basano su questo tipo di vettori: oltre alla già citata Libmeldy, anche Kymriah per leucemia linfoblastica acuta a cellule B e linfoma diffuso a grandi cellule B, Zynteglo per la beta talassemia, Skysona per l’adrenoleucodistrofiae Abecma per il mieloma multiplo (dati Osservatorio Terapie Avanzate).
Lo stesso vale per le altre tre terapie geniche nate nei laboratori dell’SR-Tiget e in corso di sperimentazione sull’uomo per sindrome di Wiskott-Aldrich, mucopolisaccaridosi di tipo 1H e beta-talassemia. A conferma della leadership a livello internazionale dell’Istituto San Raffaele-Telethon di Milano in questo campo, basti pensare che circa un terzo di tutti i pazienti con malattie genetiche coinvolti ad oggi in sperimentazioni cliniche di terapia genica con vettori lentivirali sono stati trattati proprio all’SR-Tiget (fonte Globaldata.com, agg. 13/7/2021).
I numeri dell’HIV/AIDS oggi
Quella da HIV/AIDS è una pandemia dall’impatto enorme in tutto il mondo, che purtroppo è ancora in corso nonostante gli innegabili progressi dal punto di vista delle terapie.
Secondo l’UNAIDS ad oggi sono 34,7 milioni le morti per AIDS dal 1981 (in calo del 61% dal picco del 2004), di cui 690.000 nel 2020. Sempre nel 2020 erano 37,6 milioni i sieropositivi, di cui 27.4 milioni (oltre il 70%) in terapia antiretrovirale. Per quanto riguarda invece le nuove infezioni, nel 2020 sono state 1.5 milioni: in calo (-47% dal picco del 1998), ma comunque un numero ancora significativo.
Per quanto riguarda l’Italia, l’Istituto superiore di sanità parla di oltre 71,5 mila casi di AIDS diagnosticati ad oggi, con oltre 46,3 mila morti. Nel 2020 sono state 1330 le nuove diagnosi di infezione da HIV e 352 quelle di AIDS, in netto calo rispetto al 2019 probabilmente come conseguenza delle restrizioni agli spostamenti legate all’emergenza Covid-19. Una tendenza positiva, ma che non deve assolutamente far abbassare la guardia, soprattutto fra i giovani: la fascia 25-29 anni risulta infatti quella più colpita, segno di una ridotta percezione del problema rispetto al passato.